德國柏林2024年1月12日 /美通社/ -- 德國柏林當地時間2024年1月11日,博安生物自主研發的地舒單抗注射液(BA6101和BA11021)的「國際Ⅲ期臨床完成入組暨Ⅰ期試驗結果發佈會」順利召開。該Ⅰ期臨床試驗的主要研究者Parexel International GmbH的Rainard Fuhr博士、博安生物研發總裁兼首席運營官竇昌林博士、博安生物首席醫學官周明博士與參與該項試驗的核心成員匯聚一堂,共同探討Ⅰ期臨床研究結果及本品在國際市場的應用前景,以加速推進BA6101和BA1102的國際開發進程。
BA6101和BA1102分別為地舒單抗原研藥Prolia®和Xgeva®的生物類似藥。Prolia®在全球範圍內廣泛應用於骨質疏鬆症,而Xgeva®則在全球用於實體腫瘤骨轉移和多發性骨髓瘤、骨鉅細胞瘤、高鈣血症的治療。
2022年11月,首個國產地舒單抗注射液BA6101(博優倍®)在中國率先上市,在臨床應用中獲得醫生與患者的積極反饋。2023年3月,BA1102的上市許可申請獲得國家藥品監督管理局受理,即將獲批上市。
博安生物在中國獲得地舒單抗首發優勢的同時,也積極同步推進其國際臨床和國際註冊,2020年Ⅰ期臨床試驗分別在美國和歐洲獲得批准,在歐洲進行的Ⅰ期臨床試驗(藥代動力學比對試驗)已經完成,於本次會議首次公佈;2022年Ⅲ期臨床試驗(有效性比對研究)分別在歐美日獲得批准,目前已經完成全部受試者入組。
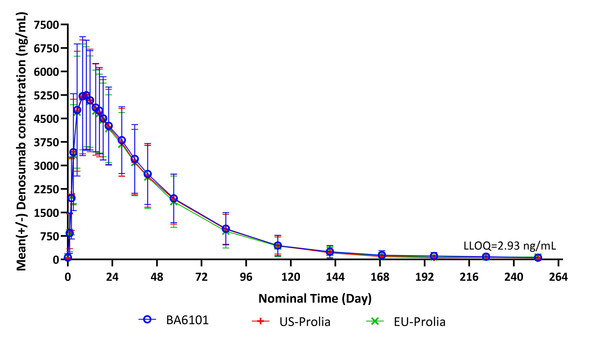
在此次柏林會議上,Ⅰ期試驗的主要研究者Rainard Fuhr博士與博安生物團隊詳細交流了臨床數據及結果。該項臨床試驗為一項隨機、雙盲、三臂、歐洲和美國來源的Prolia®對照的單次給藥比對研究。研究結果顯示:BA6101、歐盟Prolia®和美國Prolia® 3組兩兩之間分別在藥代動力學和藥效動力學達到生物等效,安全性和免疫原性相似。
Rainard Fuhr博士在會上表示:「地舒單抗在全球範圍內得到廣泛應用,並在相關治療領域中持續發揮出重要作用。生物類似藥的研發是滿足患者臨床需求的重要途徑。我們很高興地看到博安生物地舒單抗的臨床數據,顯示其國際臨床試驗的高質量推進。我們期待這兩款產品的盡快上市,為患者提供優質治療選擇,提升相關治療領域的用藥可及性。」
當前進行的地舒單抗國際多中心有效性安全性比對臨床(Ⅲ期)試驗,在歐洲、美國、日本三地同步展開。該試驗為一項隨機、雙盲、平行、原研參照藥對照的國際多中心臨床研究,比較博安生物的地舒單抗注射液與原研參照藥Prolia®的有效性、安全性、藥代動力學及免疫原性。根據美國食品藥品監督管理局(FDA)發佈的行業指南《證明與參照藥生物相似性方面的科學考慮》2、歐洲藥品監督管理局(EMA)發佈的《生物類似藥指南》3、日本醫藥品醫療器械綜合機構(PMDA)發佈的《生物類似藥的質量、安全性和有效性保證指南》4以及博安生物與FDA、EMA和PMDA的溝通交流意見,在完成國際多中心比對臨床試驗後BA6101和BA1102可分別向FDA、EMA和PMDA提交上市申請,申請原研參照藥的全部適應症。
博安生物研發總裁兼首席運營官竇昌林博士表示:「公開數據顯示Prolia®和Xgeva®在2022年的全球銷售額分別達到36.3億美元和20.1億美元,可以預見地舒單抗生物類似藥也將具有廣闊的國際市場前景。我們將在嚴格遵循國際GCP標準完成國際多中心Ⅲ期臨床試驗的同時,繼續加強全面符合歐美日要求的cGMP體系建設,為順利申報上述國家和地區的上市許可申請做好準備。」
關於博安生物
博安生物(6955.HK)是一家全面綜合性生物製藥公司,專業從事生物藥開發、生產和商業化,專注於腫瘤、自身免疫、眼科和代謝疾病。公司的新藥發現活動圍繞多個平台展開,包括全人抗體轉基因小鼠及噬菌體展示技術平台、雙特異T-cell Engager技術平台、抗體藥物偶聯(ADC)技術平台及細胞治療平台。
博安生物擁有完整的涵蓋抗體發現、細胞株開發、上游及下游工藝開發、分析及生物分析方法開發、技術轉移、非臨床研究、臨床研究、法規與註冊及商業化規模生產的全整合型產業鏈。在細胞治療領域,博安聚焦新一代增強型及可調控T細胞治療技術,研發更安全、有效、可負擔的細胞治療產品。
目前,博安生物已擁有兩款商業化產品,以及多個具有國際知識產權保護的創新型生物藥和生物類似藥的在研產品組合。除了在中國,博安生物也在包括歐美地區在內的海外市場從事生物藥產品開發。基於差異化的產品組合,以及不斷成熟的商業化能力,博安生物已構建起覆蓋「研發-生產-商業化」的全產業價值鏈運營體系,為其長期的高質量發展奠定堅實基礎。
- 備註:博安生物地舒單抗BA6101和BA1102的曾用產品代號分別為LY06006和LY01011
- FDA. Scientific Considerations in Demonstrating Biosimilarity to a Reference Product. April 2015
- EMA. Guideline on similar biological medicinal products. CHMP/437/04 Rev 1. 2015
- PMDA. Guideline for the quality, safety, and efficacy assurance of follow-on biologics. 2009